效应蛋白(Effector proteins)在病原菌-宿主相互作用中发挥着重要作用。它们通过调控宿主细胞的信号转导,免疫响应等方式,促进细菌的侵染。这些效应蛋白往往都是靶向细胞中特定的信号转导通路,并具有独特的底物识别机制和催化机理。因此,利用细菌效应蛋白调控细胞内异常的信号转导,以实现治疗性应用,具有广阔的前景。然而,目前尚缺乏有效的蛋白质胞内递送策略,限制了这些潜在的应用。近年来,阳离子脂质体介导的蛋白质胞内递送策略,凭借其高效的递送能力,吸引了研究者们的关注。
细胞内异常激活的MAPK激酶信号通路是导致包括癌症在内的多种疾病产生的重要原因。因此,抑制异常激活的MAPK信号是一种有效的癌症治疗策略,但目前临床使用的针对MAPK通路的小分子抑制剂易产生耐药性。近年来,对MAPK通路的共价抑制策略,尤其是对其终端蛋白ERK进行不可逆阻断,吸引了极大的关注。
志贺氏杆菌效应蛋白OspF能够特异地靶向宿主MAPK信号通路的终端激酶ERK,并通过一种β-消除的不可逆反应,使ERK蛋白永久失活,从而彻底阻断MAPK信号通路。 受此启发,澳门新甫京娱乐娱城平台化学与分子工程学院陈鹏教授与中国科学院化学研究所汪铭研究员合作,借助于高通量脂质体筛选策略,实现了阳离子脂质体介导的OspF胞内递送,对癌细胞MAPK信号通路和肿瘤生长进行了特异抑制,并对巨噬细胞免疫响应进行了特异调控(图1)。相关成果以“Cationic Lipid-based Intracellular Delivery of Bacterial Effectors for Rewiring Malignant Cell Signaling”为题在Angewandte Chemie International Edition杂志上发表。
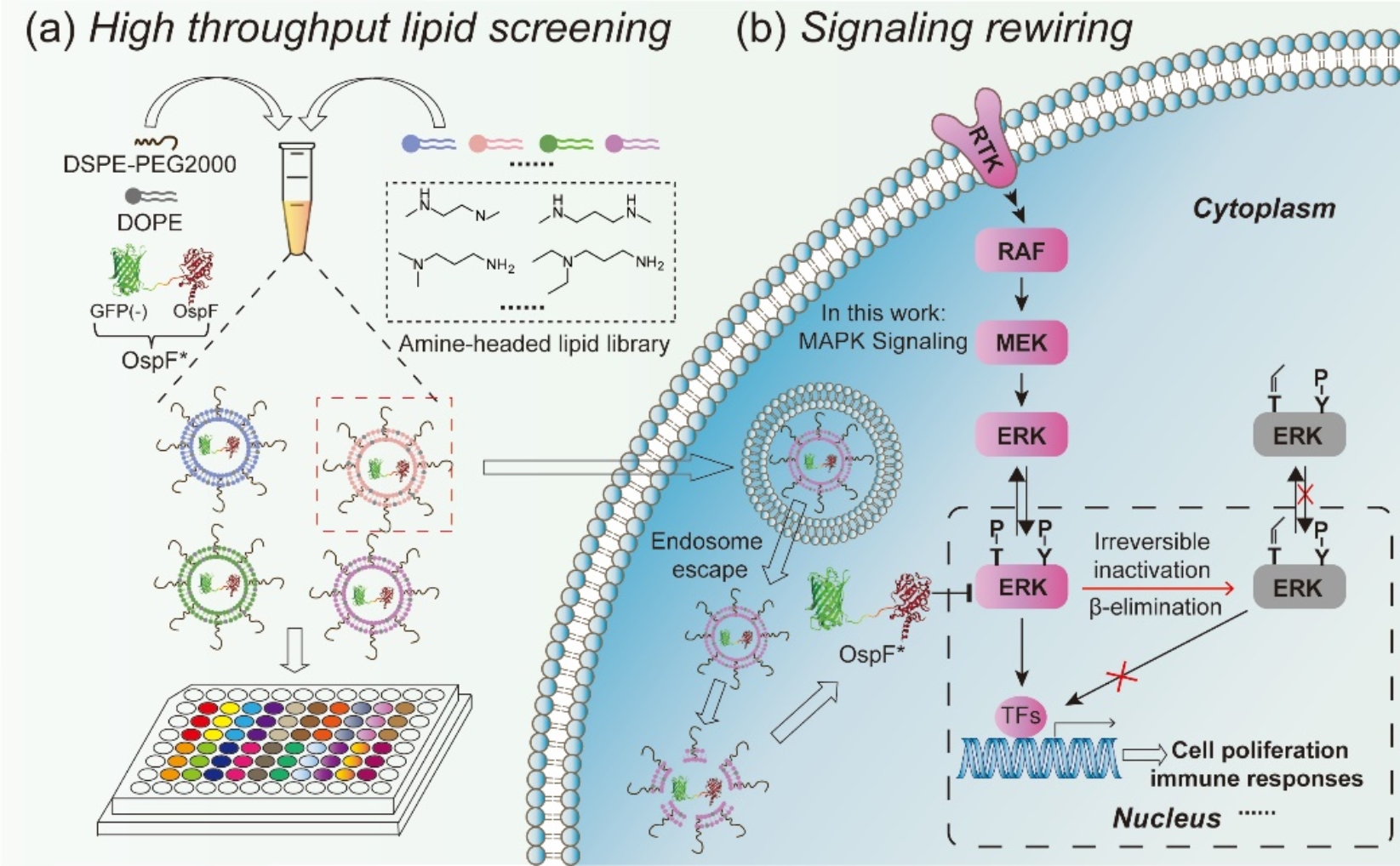
图1 细菌效应蛋白“胞内递送”的策略与应用
作者通过构建阳离子脂质体文库和基于OspF催化机理的高通量筛选平台,成功地获得了能够高效递送OspF的阳离子脂质体(图2)。细胞摄取实验证明OspF能够借助阳离子脂质体而有效地被细胞摄取。
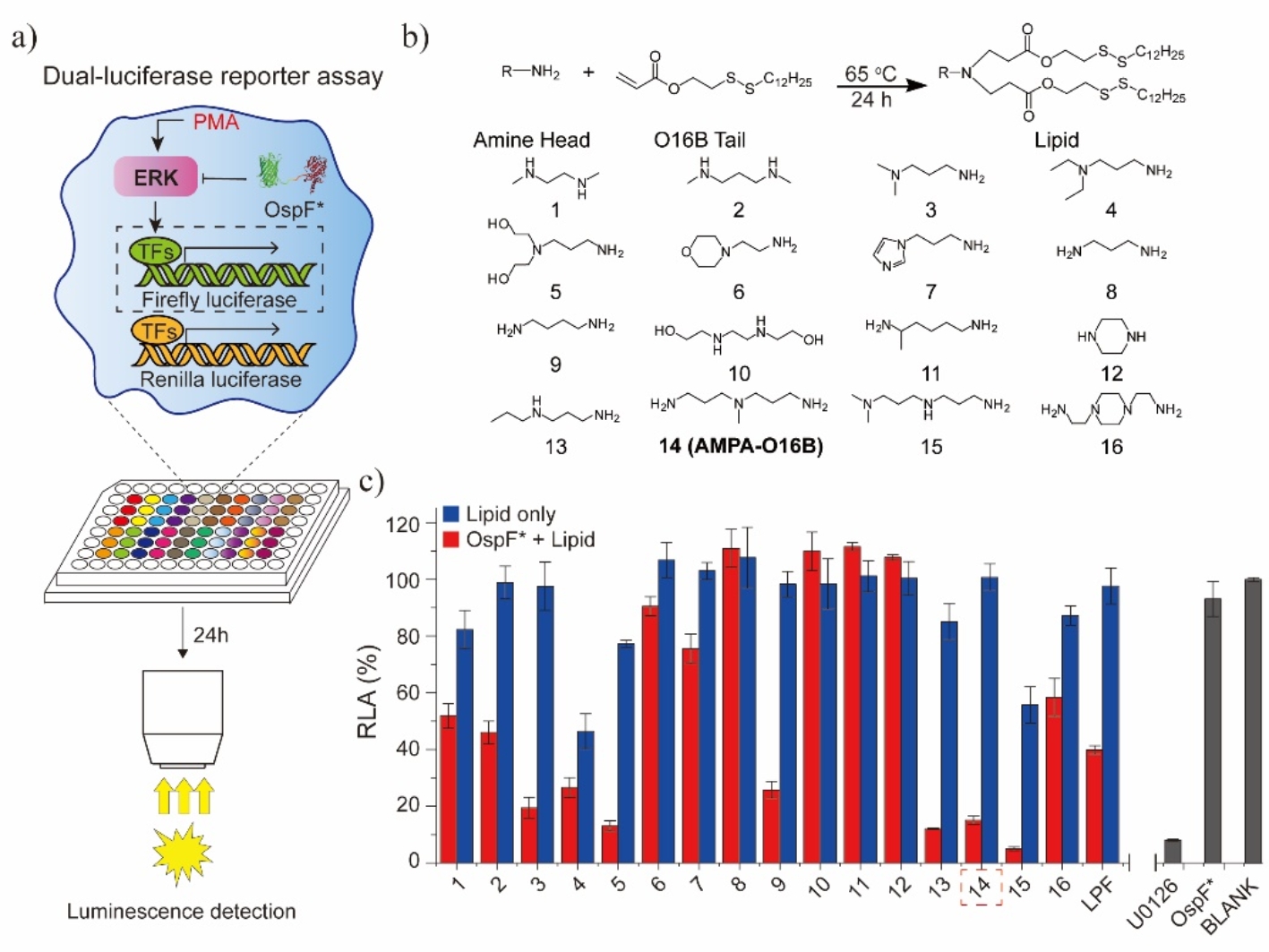
图2 基于阳离子脂质体的高通量筛选平台
接下来,作者探究了OspF对癌细胞MAPK信号的调控作用。结果表明,OspF能够在多种癌细胞中有效地抑制ERK的活性,继而阻断MAPK信号。进一步地,在小鼠肿瘤模型上,作者观察到了被阳离子脂质体递送的OspF有效地富集在肿瘤部位,并展现了有效地抑制肿瘤生长的能力(图3)。
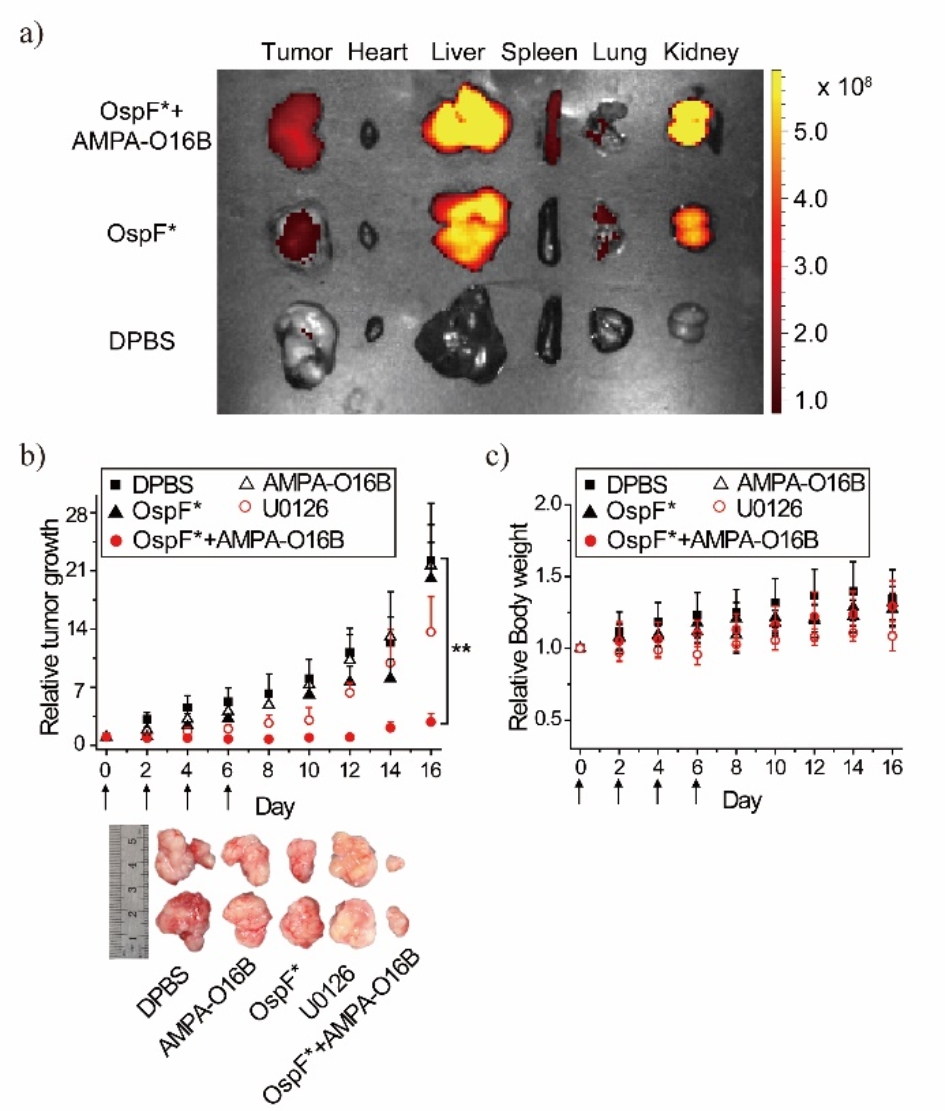
图3 胞内递送的OspF能够有效抑制肿瘤生长
最后,作者尝试利用OspF调控巨噬细胞的免疫响应。结果表明,借助于阳离子脂质体,OspF被成功地递送至巨噬细胞,并通过MAPK信号调控了巨噬细胞炎症因子释放等免疫响应(图4)。
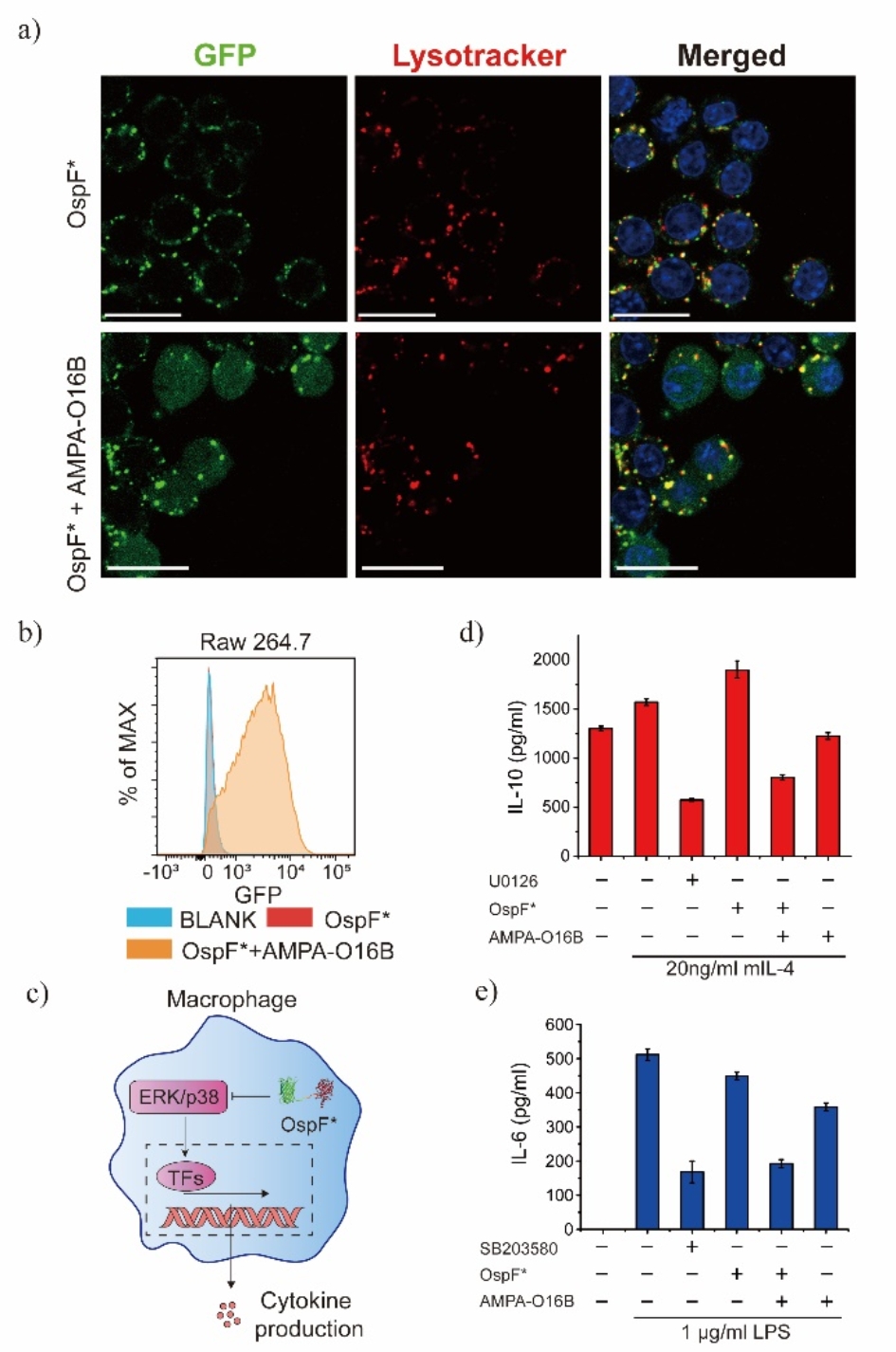
图4 OspF调控巨噬细胞免疫响应
综上,作者报导了一种阳离子脂质体介导的细菌效应蛋白胞内递送策略,用以调控癌细胞的异常信号转导,进而抑制肿瘤的生长。同样的策略还可以被用于巨噬细胞等难以转染的免疫细胞类型。该工作为深入挖掘细菌天然效应蛋白在疾病治疗等方面的潜力,提供了一种普适性的策略。
论文的共同第一作者为澳门新甫京娱乐娱城平台博士研究生杨绍君和中国科学院化学研究所硕士研究生唐巧;陈鹏教授与汪铭研究员为共同通讯作者。该工作得到了国家自然科学基金委、科技部、北京分子科学国家研究中心以及北大-清华生命科学联合中心的资助。
论文链接: https://www.onlinelibrary.wiley.com/doi/epdf/10.1002/anie.202009572
DOI: 10.1002/anie.202009572 and 10.1002/ange.202009572